
��Ŀ�� ��Դ�� �}�ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
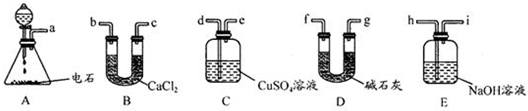
| HBr |
| ���� |
| ����a |
| NaOH��Һ |
| �� |
| ����b |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
| �ܽ� |
| �� |
| �� |
| �� |
| �^�V |
| �� |
| �m���}�� |
| �� |
| ���l(f��)�p�Y(ji��)���p��� |
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
2- 4 |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
| ��(y��ng)�Q��NaOH���|(zh��)��/g | ��(y��ng)�x������ƿ��Ҏ(gu��)��/mL | ������ƿ��߀��Ҫ�������x�� |
�鿴�𰸺ͽ���>>
�ٶ����� - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com