
題目列表(包括答案和解析)
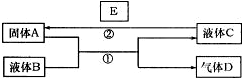 (2007?淄博三模)中學化學中有很多物質可以實現下圖中物質之間的轉化.其中反應條件和部分反應的產物已略去.液體B和C可能是單一溶質的溶液,也可能是純凈物.
(2007?淄博三模)中學化學中有很多物質可以實現下圖中物質之間的轉化.其中反應條件和部分反應的產物已略去.液體B和C可能是單一溶質的溶液,也可能是純凈物.
| ||
| ||

| ||
| ||
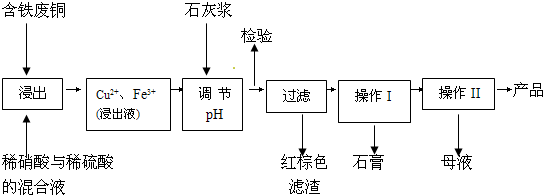
| 溫度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 膽礬 | 32 | 44.6 | 61.8 | 83.8 | 114 |
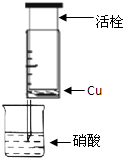 某研究性學習小組設計不同實驗方案來研究硝酸的性質.
某研究性學習小組設計不同實驗方案來研究硝酸的性質.| 組 | m(Cu)/g | 硝酸(過量) | 溶液顏色 |
| A | 1 | 濃HNO3(4mL) | 溶液為綠色 |
| 1 | 稀HNO3(4mL) | 溶液為藍色 | |
| B | 0.5 | 濃HNO3(4mL) | 溶液為綠色 |
| 1 | 稀HNO3(4mL) | 溶液為藍色 | |
| C | 2 | 濃HNO3(4mL) | 溶液為綠色 |
| 1 | 稀HNO3(4mL) | 溶液為藍色 |
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com