
�}Ŀ�б�(�����𰸺ͽ���)
| ��x��/kJ?mol-1 | I1 | I2 | I3 | I4 |
| X | 496 | 4562 | 6912 | 9543 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 578 | 1817 | 2745 | 11578 |
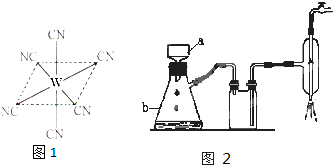
| ���Wʽ | Fe | FeO | Fe2O3 | Fe3O4 | Fe��OH��2 | Fe��OH��3 |
| �ɫ | �y��ɫ | ��ɫ | �tɫ | ��ɫ | ��ɫ | �t��ɫ |
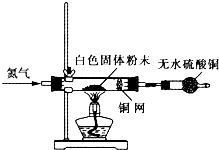
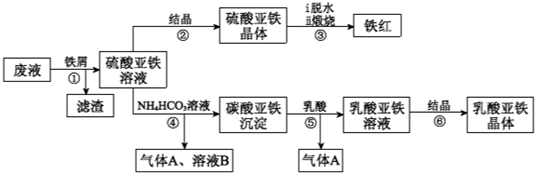
| 13.9 |
| a |
| 13.9 |
| a |

| 2 |
| 3 |
| 2 |
| 3 |
| ||
| ||
| �ض�/�� | 10 | 20 | 30 | 40 | 50 | 70 |
| ��NH4��2SO4 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
| FeSO4?7H2O | 40.0 | 48.0 | 60.0 | 73.3 | - | - |
| ��NH4��2Fe��SO4��2?6H2O | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
| 1 |
| V |
| 1 |
| V |
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com