
��Ŀ�� ��Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
 CH3COOC2H5+H2O��
CH3COOC2H5+H2O���鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}

| A�� | C20H12 | B�� | C20H34 | C�� | C22H12 | D�� | C30H36 |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | 20 mL 3mol/L | B�� | 20 mL 2 mol/L | C�� | 10 mL 4 mol/L | D�� | 10 mL 2 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
 ��(sh��)�(y��n)С�Mͬ�W(xu��)����һ�t��(b��o)����ij�켈�S�`����܇��Ư��Һ��NaCl��NaClO�Ļ��Һ������ʢ���KAl��SO4��2��Һ�ij��У�����ж��¼���ԓС�Mͬ�W(xu��)��̽���ж�ԭ���M(j��n)��������(sh��)�(y��n)��
��(sh��)�(y��n)С�Mͬ�W(xu��)����һ�t��(b��o)����ij�켈�S�`����܇��Ư��Һ��NaCl��NaClO�Ļ��Һ������ʢ���KAl��SO4��2��Һ�ij��У�����ж��¼���ԓС�Mͬ�W(xu��)��̽���ж�ԭ���M(j��n)��������(sh��)�(y��n)���鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}

 ��
���鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | �������x�ӵ����ʽ�� 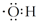 | |
| B�� | ������̼���ӵı���ģ����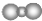 | |
| C�� | ����N�ĽM��ͨʽ��CnH2n-6��n��6�� | |
| D�� | 12C��14C��ԭ�ӽY(ji��)��(g��u)ʾ��D���ɱ�ʾ�� 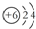 |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ��2016-2017�W(xu��)���|����ꖖ|�����ŌW(xu��)У��һ�A�ο�һ���W(xu��)���������棩 �}�ͣ��x���}
��������һ�����|(zh��)�����ĝ�ȵ���Һ�Č��Ãx�� ��ʹ��ǰҪ�șz������ƿ�Ƿ�©Һ ������ƿ�����Á��ӟ� �ܲ���������ƿ�A�����ƺõ���Һ �ݿ�����500mL����ƿ����250mL��Һ��
A. �ٺ͢� B. �ٺ͢� C. ���ˢ� D. ���ˢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
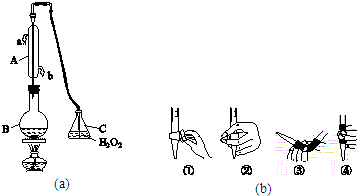
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}

| A�� | �VҺA�в���F(xi��n)e3+ | |
| B�� | ��Ʒ�к���Ԫ�ص����|(zh��)������0.01mol | |
| C�� | �ψD��V=112 | |
| D�� | �ܽ��Ʒ���^�������ĵ�����Ŀ������|(zh��)������0.02mol |
�鿴�𰸺ͽ���>>
�ٶ����� - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com